
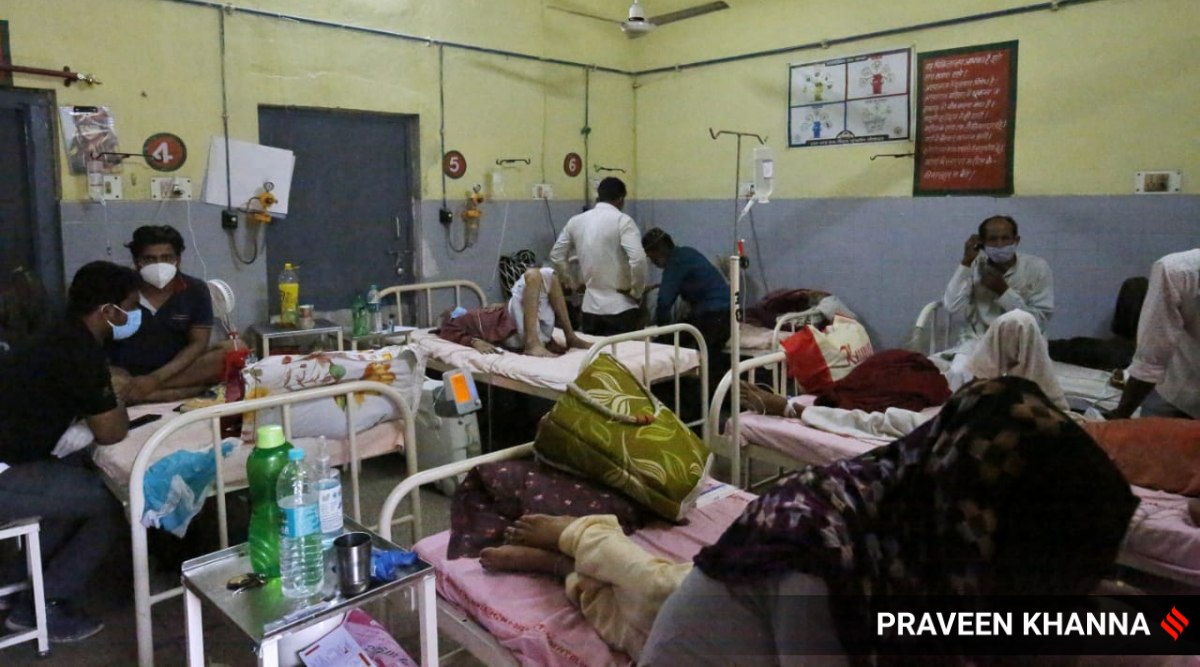
 Familieleden die voor Covid-patiënten zorgen in de Covid-isolatieafdeling van het districtsziekenhuis Muzaffarnagar in Uttar Pradesh.
Familieleden die voor Covid-patiënten zorgen in de Covid-isolatieafdeling van het districtsziekenhuis Muzaffarnagar in Uttar Pradesh.
Een door de DRDO ontwikkeld anti-COVID-medicijn is door de Drugs Controller General of India (DCGI) goedgekeurd voor gebruik in noodgevallen als aanvullende therapie bij matige tot ernstige coronaviruspatiënten, zei het ministerie van Defensie op zaterdag.
Klinische onderzoeken met het medicijn 2-deoxy-D-glucose (2-DG) toonden aan dat het helpt bij een sneller herstel van gehospitaliseerde patiënten en de aanvullende zuurstofafhankelijkheid vermindert, zei het.
De goedkeuring voor het medicijn is gekomen in een tijd waarin India worstelt met een recordbrekende golf van coronavirus-pandemie die de gezondheidszorginfrastructuur van het land tot het uiterste heeft opgerekt.
https://images.indianexpress.com/2020/08/1×1.png
& # 8220; In de aan de gang zijnde tweede COVID-19-golf wordt een groot aantal patiënten geconfronteerd met ernstige zuurstofafhankelijkheid en hebben ze ziekenhuisopname nodig.
Topnieuws op dit moment
Klik hier voor meer
& # 8220; Het medicijn zal naar verwachting kostbare levens redden vanwege het werkingsmechanisme van het medicijn in geïnfecteerde cellen. Dit vermindert ook de opnameduur van COVID-19-patiënten, & # 8221; zei het ministerie.
Het zei dat de anti-COVID-19 therapeutische toepassing van 2-DG-medicijn is ontwikkeld door het Institute of Nuclear Medicine and Allied Sciences (INMAS), een toonaangevend laboratorium van de Defense Research and Development Organization (DRDO), in samenwerking met Dr Reddy & # 8217; s Laboratories (DRL) in Hyderabad.
& # 8220; Op 1 mei verleende DCGI toestemming voor het gebruik van dit medicijn in noodgevallen als aanvullende therapie bij matige tot ernstige COVID-19-patiënten. Omdat het een generiek molecuul en analoog van glucose is, kan het gemakkelijk in het hele land worden geproduceerd en beschikbaar worden gesteld, & # 8221; zei het ministerie in een verklaring.
Adjuvante therapie is een behandeling die samen met de primaire behandeling wordt gebruikt om haar te ondersteunen.
Het medicijn komt in poedervorm in een sachet en wordt oraal ingenomen door het lost het op in water.
& # 8220; Het hoopt zich op in de met virus geïnfecteerde cellen en voorkomt virusgroei door de virale synthese en energieproductie te stoppen. De selectieve accumulatie in viraal geïnfecteerde cellen maakt dit medicijn uniek, & # 8221; zei het ministerie.
In termen van werkzaamheidstrends, zei het ministerie, vertoonden patiënten die met 2-DG werden behandeld een snellere symptomatische genezing dan de standaardzorg (SoC) op verschillende eindpunten.
& # 8220; Een significant gunstige trend (2,5 dagen) verschil) werd gezien in termen van de mediane tijd tot het bereiken van normalisatie van specifieke parameters voor vitale functies in vergelijking met SoC, & # 8221; zei het.
& # 8220; Resultaten van klinische onderzoeken van het medicijn hebben aangetoond dat het helpt bij het sneller herstel van gehospitaliseerde patiënten en de aanvullende zuurstofafhankelijkheid vermindert. Een groter deel van de met 2-DG behandelde patiënten vertoonde RT-PCR-negatieve conversie bij COVID-patiënten & # 8221; het toegevoegd.
Het ministerie zei dat het medicijn een enorm voordeel zal hebben voor de mensen die aan COVID-19 lijden.
Het zei dat de DRDO aan het project begon na premier Narendra Modi & # 8217; s pleidooi voor paraatheid tegen de pandemie begin vorig jaar.
& # 8220; In april 2020, tijdens de eerste golf van de pandemie, voerden INMAS-DRDO-wetenschappers laboratoriumexperimenten uit met de hulp van het Centrum voor Cellulaire en Moleculaire Biologie, Hyderabad en ontdekten dat dit molecuul effectief werkt tegen het SARS-CoV-2-virus en remt de virale groei, & # 8221; zei het ministerie.
Op basis van deze resultaten heeft de Central Drugs Standard Control Organization (CDSCO) van de DCGI in mei 2020 een Fase-II klinische studie van 2-DG bij COVID-19-patiënten toegestaan./p>
Het ministerie zei dat de DRDO, samen met DRL, de klinische onderzoeken is gestart om de veiligheid en werkzaamheid van het medicijn bij COVID-19-patiënten te testen.
& # 8220; In fase II-onderzoeken uitgevoerd in de periode mei tot oktober 2020 , bleek het medicijn veilig te zijn bij COVID-19-patiënten en vertoonde het een significante verbetering in hun herstel, & # 8221; zei het.
& # 8220; Fase IIa werd uitgevoerd in zes ziekenhuizen en fase IIb (dosisbereik) klinische studie werd uitgevoerd in 11 ziekenhuizen in het hele land. Fase II-studie werd uitgevoerd bij 110 patiënten, & # 8221; zei het.
Het ministerie zei op basis van succesvolle resultaten dat DCGI de klinische fase III-studie in november 2020 verder toestond.
Het zei dat de klinische fase-III-studie tussen december 2020 en maart 2021 bij COVID 27 werd uitgevoerd bij 220 patiënten. ziekenhuizen in Delhi, Uttar Pradesh, West-Bengalen, Gujarat, Rajasthan, Maharashtra, Andhra Pradesh, Telangana, Karnataka en Tamil Nadu.
& # 8220; De gedetailleerde gegevens van de klinische fase III-studie werden gepresenteerd aan DCGI. In de 2-DG-arm verbeterde een significant groter deel van de patiënten symptomatisch en werden ze op dag 3 vrij van aanvullende zuurstofafhankelijkheid (42 procent versus 31 procent) in vergelijking met SoC, wat wijst op een vroege verlichting van zuurstoftherapie/-afhankelijkheid, & # 8221; zei het ministerie.
& # 8220; De vergelijkbare trend werd waargenomen bij patiënten ouder dan 65 jaar & # 8221; stond er.
-
- De Indian Express-website is GROEN beoordeeld vanwege zijn geloofwaardigheid en betrouwbaarheid door Newsguard, een wereldwijde service die nieuwsbronnen beoordeelt op hun journalistieke normen.
-



