
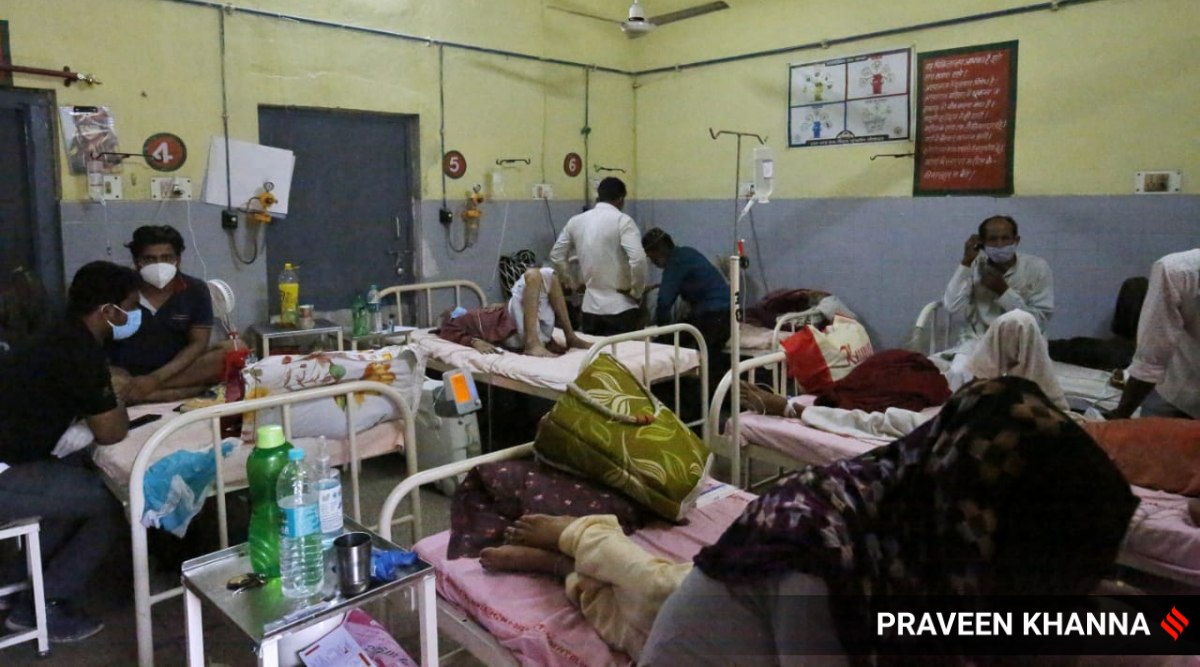
 Familjemedlemmar som tar hand om Covid-patienter på Covids isoleringsavdelning vid Muzaffarnagar distriktssjukhus i Uttar Pradesh.
Familjemedlemmar som tar hand om Covid-patienter på Covids isoleringsavdelning vid Muzaffarnagar distriktssjukhus i Uttar Pradesh.
Ett oralt anti-COVID-läkemedel som utvecklats av DRDO har godkänts av Drugs Controller General of India (DCGI) för akut användning som kompletterande behandling för måttliga till svåra coronaviruspatienter, sade försvarsministeriet på lördag.
Kliniska prövningar av läkemedlet 2-deoxi-D-glukos (2-DG) visade att det hjälper till med snabbare återhämtning av sjukhuspatienter och minskar extra syreberoende, säger det.
Godkännandet av läkemedlet har kommit i en tid då Indien har kämpat med en rekordbrytande våg av koronaviruspandemi som har sträckt landets hälsoinfrastruktur till sin gräns.
https://images.indianexpress.com/2020/08/1×1.png
& # 8220; I den pågående andra COVID-19-vågen står ett stort antal patienter inför svårt syreberoende och behöver sjukhusvistelse.
Toppnyheter just nu
Klicka här för mer
& # 8220; Läkemedlet förväntas rädda värdefulla liv på grund av läkemedlets funktion i infekterade celler. Detta minskar också sjukhusvistelsen för COVID-19-patienter, & # 8221; sa ministeriet.
Det sägs att den terapeutiska tillämpningen av 2-DG-läkemedlet mot COVID-19 har utvecklats av Institute of Nuclear Medicine and Allied Sciences (INMAS), ett ledande laboratorium för Defense Research and Development Organization (DRDO), i samarbete med Dr Reddy & # 8217; s Laboratories (DRL) i Hyderabad.
& # 8220; Den 1 maj beviljade DCGI tillstånd för akut användning av detta läkemedel som tilläggsbehandling hos måttliga till svåra COVID-19-patienter. Eftersom det är en generisk molekyl och analog av glukos, kan den lätt produceras och göras tillgänglig i gott om i landet, & # 8221; sade ministeriet i ett uttalande.
Tilläggsbehandling är en behandling som används tillsammans med den primära behandlingen för att hjälpa den.
Läkemedlet kommer i pulverform i en påse och tas oralt av lösa det i vatten.
& # 8220; Det ackumuleras i de virusinfekterade cellerna och förhindrar virustillväxt genom att stoppa virussyntes och energiproduktion. Dess selektiva ansamling i virusinfekterade celler gör detta läkemedel unikt, & # 8221; sa ministeriet.
När det gäller effekttrender, sade ministeriet, visade patienter som behandlades med 2-DG snabbare symtomatisk botning än vårdstandarden (SoC) på olika slutpunkter.
& # 8220; En betydligt gynnsam trend (2,5 dagar skillnad) sågs i termer av mediantiden för att uppnå normalisering av specifika parametrar för vitala tecken jämfört med SoC, & # 8221; stod det.
& # 8220; Kliniska prövningsresultat av läkemedlet har visat att det hjälper till med snabbare återhämtning av sjukhuspatienter och minskar extra syreberoende. En högre andel patienter som behandlades med 2-DG visade RT-PCR-negativ omvandling hos COVID-patienter, & # 8221; tillade det.
Ministeriet sa att läkemedlet kommer att vara till stor nytta för de människor som lider av COVID-19. # 8217; s krav på beredskap mot pandemin i början av förra året.
& # 8220; I april 2020, under den första vågen av pandemin, genomförde INMAS-DRDO-forskare laboratorieexperiment med hjälp av Center for Cellular and Molecular Biology, Hyderabad och fann att denna molekyl fungerar effektivt mot SARS-CoV-2-virus och hämmar virustillväxten, & # 8221; sade ministeriet.
Baserat på dessa resultat tillät DCGI: s Central Drugs Standard Control Organization (CDSCO) fas II-klinisk prövning av 2-DG hos COVID-19-patienter i maj 2020.
Ministeriet sa att DRDO, tillsammans med DRL, påbörjade de kliniska prövningarna för att testa läkemedlets säkerhet och effekt hos COVID-19-patienter.
& # 8220; I fas II-studier genomförda under maj till oktober 2020 , visade sig läkemedlet vara säkert hos COVID-19-patienter och visade signifikant förbättring av deras återhämtning, & # 8221; stod det.
& # 8220; Fas IIa genomfördes på sex sjukhus och klinisk fas IIb (dosintervall) genomfördes på 11 sjukhus över hela landet. Fas-II-försök utfördes på 110 patienter, & # 8221; stod det.
Ministeriet sa att baserat på framgångsrika resultat tillät DCGI vidare klinisk fas-III-studie i november 2020.
Det sa att klinisk fas-III-studie genomfördes på 220 patienter mellan december 2020 och mars 2021 vid 27 COVID sjukhus i Delhi, Uttar Pradesh, Västbengalen, Gujarat, Rajasthan, Maharashtra, Andhra Pradesh, Telangana, Karnataka och Tamil Nadu.
& # 8220; De detaljerade uppgifterna från klinisk fas-III-studie presenterades för DCGI. I 2-DG-armen förbättrades en signifikant högre andel patienter symtomatiskt och blev fria från kompletterande syreberoende (42 procent mot 31 procent) vid dag 3 jämfört med SoC, vilket indikerar en tidig lindring från syrebehandling/beroende, & # 8221; sade ministeriet.
& # 8220; Den liknande trenden observerades hos patienter över 65 år, & # 8221; stod det.
-
- Indian Express-webbplatsen har varit betygsatt GRÖNT för sin trovärdighet och pålitlighet av Newsguard, en global tjänst som betygsätter nyhetskällor för deras journalistiska standarder.
-



